Водневий зв'язок.
Водневий зв'язок - зв'язок між позитивно зарядженим атомом водню однієї молекули і негативно зарядженим атомом іншої молекули.
Механізм виникнення водневого зв'язку - частково електростатичний і частково донорно-акцепторні.
Характерною рисою водневого зв'язку є відстань між атомом водню і іншим атомом, її створює. Воно повинно бути менше, ніж сума радіусів цих атомів.
Воднева зв'язок підрозділяється:
1. Міжмолекулярна воднева зв'язок утворюється між молекулами речовин, до складу яких входять водень і сильно електронегативний елемент - фтор , кисень , Азот, хлор , сірка . Сильно зміщена загальна електронна пара від водню до атома негативно зарядженого елемента, при цьому позитивний заряд водню сконцентрований в малому обсязі, призводить взаємодія протона з неподіленої електронної парою іншого атома або іона, обобществляя її.
Водневий зв'язок позначають точками, вказуючи, що вона набагато слабкіше ковалентної зв'язку (приблизно в 15-20 разів).
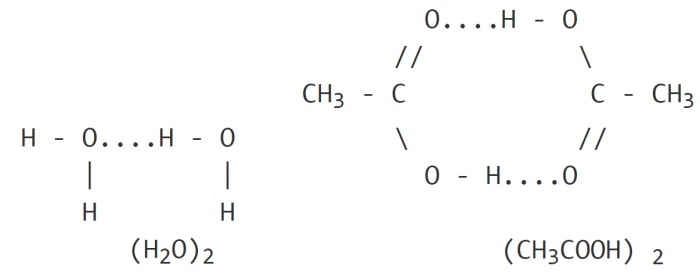
Межмолекулярная воднева зв'язок: дві молекули води і дві молекули оцтової кислоти з утворенням циклічної структури
2. внутрішньомолекулярного водневого зв'язок присутній в багатоатомних спиртах, вуглеводах, білках і інших органічних речовинах.
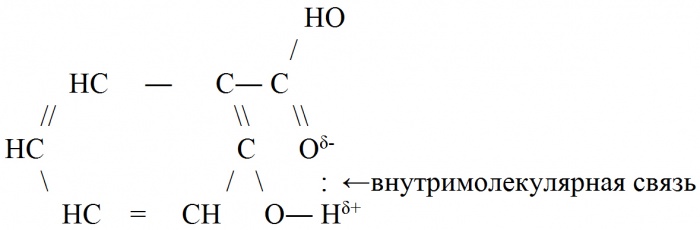
Молекула саліцилової кислоти.
Речовини з водневої зв'язок мають молекулярні кристалічні решітки, у вузлах якої знаходяться молекули.
приклади: вода у вигляді льоду, йод , Хлор, бром , «Сухий лід» (твердий діоксид вуглецю ), Твердий аміак, а також тверді органічні речовини (метан, бензол, фенол, нафталін, білки і т.д.).
Воднева зв'язок забезпечує низькомолекулярних речовин здатність бути при звичайних умовах в рідкому агрегатному стані (етанол, метанол, вода) або зріджують газами (аміак, фтороводород).
Більш висока температура кипіння води (100 оС) в порівнянні з водневими сполуками елементів підгрупи кисню (Н2S, Н2Sе, Н2Те), так як витрачається додаткова енергія на руйнування водневих зв'язків.
Також під час плавлення води її щільність зростає. Це пояснюється тим, що в структурі льоду кожен атом кисню пов'язаний через атоми водню з чотирма іншими атомами кисню інших молекул води. В результаті утворюється пухка «ажурна» структура.
